细菌内毒素检测:选择重组 C 因子方法的 10 个理由
重组鲎因子 C(rFC) 法是最有效细菌内毒素检测 (BET) 的最新最先进的解决方案。该白皮书 回顾了与当前广泛使用的 BET 法相比, 重组鲎因子 C(rFC) 的优势。我们比较了 LAL 试剂和 rFC 的性能,并总结了我司选择 rFC 的 10 个 理由。
背景
作为一种免疫细胞,巨噬细胞使用构成革兰氏阴性菌外细胞壁的脂多糖 (LPS) 分子来检测体内是否存在内毒素。LPS,也称为细菌内毒素,可引起严重的免疫系统应答,发热、低血压、恶心、休克和败血症。
人体对细菌内毒素的严重反应可能致命,我们必须非常小心得对待内毒素以确保其不会进入与患者血流或脑血流接触的医疗产品1,2。遗憾的是避免制药工艺中的内毒素污染绝非易事,因为环境中基本到处都有 LPS 分子,所以对可能接触患者血液或脑液的医疗器械、 注射药物以及其他医疗溶液中内毒素污染的可接受水平有严格的规定,此类产品在放行前必须进行内毒素污染检测3。
使用 LAL 进行内毒素检测的简史
20 世纪 60 年代,科学家发现大西洋鲎的分离裂解物(大西洋鲎阿米巴细胞裂解物——LAL)可在存在细菌内毒素的情况下凝结。大约 10 年后, 研究人员还发现,亚洲鲎的分离裂解物(亚洲鲎阿米巴细胞裂解物——TAL)也出现了同样的情况。受到上述发现的鼓舞,研究人员开发了一项使用 LAL 和 TAL 试剂检测细菌内毒素的检测,1983 年该方法被美国药典采用2,4。
有三种获批的主要检测方法使用 LAL 和 TAL 试剂检测内毒素:凝胶法(限度 和半定量)、比浊法和显色(终点和动力学法)含量测定。LAL/TAL 的所有检测原理都类似;样品中细菌内毒素引发一连串的反应,导致浊度或颜色的变化(见图 1)4,5。
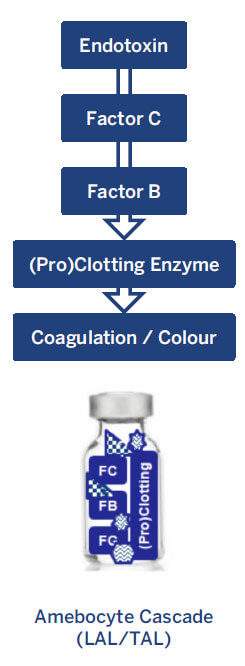 阿米巴细胞裂解物含有一种天然蛋白质混合物,该类蛋白质会参与内毒素 检测过程。因子 C 通过与 细菌内毒素结合并激活 另一种称为因子 B 的蛋白质的方式充当着主要生物传感器的角色。然后因子B将凝固酶原转化为凝固酶。产生的凝固酶然后催化导致 粘度、浊度或颜色变化的反应,检测该反应以确定样品中内毒素的浓度4,5。
阿米巴细胞裂解物含有一种天然蛋白质混合物,该类蛋白质会参与内毒素 检测过程。因子 C 通过与 细菌内毒素结合并激活 另一种称为因子 B 的蛋白质的方式充当着主要生物传感器的角色。然后因子B将凝固酶原转化为凝固酶。产生的凝固酶然后催化导致 粘度、浊度或颜色变化的反应,检测该反应以确定样品中内毒素的浓度4,5。
LAL:环境影响和限制
虽然 LAL 和 TAL 广泛用于制药工业(主要是因其可达到内毒素检测的灵敏度要求),但其存在如下几个 缺点。LAL 和 TAL 检测容易出现假阳性;天然裂解物试剂的 批间差异较大, 降低了其可靠性和可比性4,6。
也许 LAL 和 TAL 试剂最大的问题是必须从鲎中提取。在过去的 15 年里, 大西洋鲎的数量减少了 90%,并且 IUCN (国际自然保护联盟)的濒危物种红色名录将该物种描述为易危物种。亚洲鲎也 受到了类似的影响,并且目前被认为是 濒危物种6,7。
随着药品销量和生产的 持续增长,内毒素检测试剂的需求也在不断增长。鲎的数量减少意味着无法持续使用 LAL 和 TAL 试剂检测细菌内毒素。此外,LAL 和 TAL 仅在某些地区生产, 因此只能在全球某些地区才能获得这些试剂6。
为了持续确保药品安全, 显然我们需要一种替代内毒素检测方法,这种方法不仅可持续,而且可广泛使用, 并能够满足不断增长的内毒素检测需求。