TEST D'ENDOTOXINE BACTÉRIENNE : 10 raisons de choisir le facteur C recombinant
Les méthodes du facteur C recombinant de limule (rFC) représentent la dernière solution de pointe pour tester efficacement les endotoxines bactériennes (BET). Ce livre blanc examine les avantages du facteur C recombinant de limule (rFC) par rapport aux méthodes BET actuellement largement utilisées. Nous comparons les performances des réactifs LAL avec les rFC et résumons les preuves justifiant nos 10 raisons de choisir le rFC.
HISTORIQUE
Les macrophages, un type de cellule immunitaire, utilisent les molécules de lipopolysaccharides (LPS) composant la paroi cellulaire externe des bactéries à Gram négatif pour détecter leur présence dans le corps. Les LPS, également connues sous le nom d'endotoxines bactériennes, peuvent provoquer une forte réponse du système immunitaire, manifestée par de la fièvre, une hypotension, des nausées, un état de choc et une septicémie.
Les endotoxines bactériennes peuvent provoquer des réactions sévères et mortelles et, à ce titre, il faut veiller à ce qu'elles ne se retrouvent pas dans les produits médicaux entrant en contact avec le sang ou le liquide cérébral d'un patient1,2. Malheureusement, éviter la contamination par les endotoxines pendant les processus de fabrication pharmaceutique n'a rien de facile, car les molécules LPS sont présentes dans pratiquement tous les environnements. En conséquence, les niveaux acceptables de contamination par les endotoxines sont strictement réglementés dans les dispositifs médicaux , les produits pharmaceutiques injectables et d'autres solutions médicales
susceptibles d'entrer en contact avec le sang ou le liquide cérébral d'un patient. De tels produits doivent, par conséquent, faire l'objet de tests pour s'assurer de l'absence de contamination en endotoxines avant de pouvoir être libérés3.
UN BREF HISTORIQUE DES TESTS LAL DE DÉTECTION D'ENDOTOXINE
Dans les années 1960, les scientifiques ont découvert que le l'hémolymphe du limule de l'Atlantique ( Limulus AmebocyteLysate -LAL) se coagulait en présence d'endotoxines bactériennes. Environ 10 ans plus tard, les chercheurs ont également découvert le même phénomène avec le lysat issu du limule asiatique (Tachypleus Amebocyte Lysate - TAL). Forts de leur découverte, ils mettent au point des tests visant à détecter les endotoxines bactériennes à l'aide des réactifs LAL et TAL, ensuite adoptés par la pharmacopée américaine en 19832,4.
Trois principales méthodologies de test approuvées utilisent les réactifs LAL et TAL pour les tests d'endotoxines : Gélification (essais limite et semi-quantitatif), turbidimétrie cinétique et chromogénique (méthodes en point final et cinétique chromogène). Les tests LAL/TAL ont un fonctionnement similaire : la présence d'endotoxines bactériennes dans un échantillon déclenche une cascade de réactions et une apparition de turbidité ou de couleur (voir Figure 1)4,5.
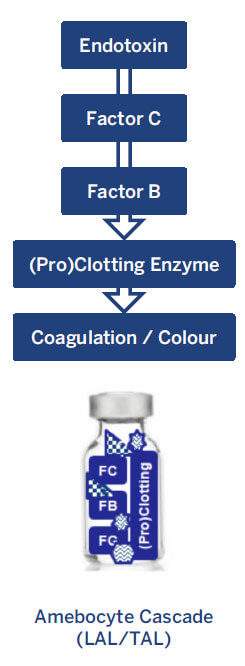 Le lysat d'amoebocytes contient un mélange de protéines d'origine naturelle impliquées dans la détection des endotoxines. Le facteur C sert de biocapteur principal en se liant aux endotoxines bactériennes et en activant une autre protéine appelée facteur B. Le facteur B convertit ensuite une enzyme pro-coagulante en une enzyme de coagulation.
Le lysat d'amoebocytes contient un mélange de protéines d'origine naturelle impliquées dans la détection des endotoxines. Le facteur C sert de biocapteur principal en se liant aux endotoxines bactériennes et en activant une autre protéine appelée facteur B. Le facteur B convertit ensuite une enzyme pro-coagulante en une enzyme de coagulation.
L'enzyme de coagulation obtenu catalyse alors une réaction qui produit un gel, de la turbidité ou
l'appartion d'une couleur. Une fois détectée, cette modification permettra de déterminer la concentration d'endotoxines dans l'échantillon4,5.
LAL : LIMITATIONS ET IMPACTS ENVIRONNEMENTAUX
Bien que largement utilisés dans l' industrie pharmaceutique (principalement parce qu'ils permettent une détection sensible des endotoxines), les tests LAL et TAL possèdent cependant plusieurs inconvénients. Ils présentent un risque de faux positifs, sans compter que les variations relativement élevées entre les lots de réactifs de lysats naturels mettent à mal leur fiabilité et leur comparabilité4,6.
Mais le principal problème des réactifs LAL et TAL vient sûrement du fait qu'ils doivent être extraits des
limules. La population de limules de l'Atlantique a diminué de 90 % au cours des 15 dernières années et l'espèce apparaît maintenant dans la catégorie "Vulnérable" de la liste rouge des espèces menacées de l'IUCN. La population de limules asiatiques a subi le même sort et appartient désormais à la catégorie "En danger6,7".
Alors que les ventes et la fabrication de produits pharmaceutiques continuent leur progression, la demande de réactifs pour les tests d'endotoxines augmente aussi . La baisse du nombre de limules signifie que l'utilisation des LAL et TAL pour tester les endotoxines bactériennes n'est plus durable. De plus, les LAL et TAL ne sont produits que dans certaines régions et leur disponibilité est donc limitée à certaines zones du globe6.
Pour maintenir la sécurité de nos produits pharmaceutiques, nous avons clairement besoin d'un test d'endotoxines alternatif qui soit non seulement durable, mais aussi largement disponible et capable de répondre aux demandes croissantes de tests d'endotoxines.